Medikamentöse HIV-Therapie und -Prävention mit langwirksamen Substanzen

von Dr. med. Sebastian Noe
Wenn man über „langwirksame“ Therapien spricht, so geht es nicht darum, dass andere HIV-Therapien nicht „langwirksam“ im Sinne von „über viele Jahr effektiv“ wären. Vielmehr geht es darum, wie häufig man ein Medikament anwenden muss, damit es wirksame Konzentrationen der antiretroviralen Substanzen aufrechterhält. Oder anders gesagt: Wie häufig muss ein Medikament genommen werden, damit es auf Dauer zuverlässig wirkt?
Es gibt keine einheitliche Definition, ab welchem Zeitabstand zwischen zwei Dosen eines Medikamentes dieses als „langwirksam“ gilt, wenn man über Strategien zur Prävention oder Therapie von HIV spricht. Üblicherweise werden unter diesem Sammelbegriff aktuell vor allem Präparate zusammengefasst, die mit einem Anwendungsintervall von einigen Wochen bis Monaten auskommen; dennoch können hierunter im weitesten Sinne auch andere Substanzen verstanden werden, die nicht täglich angewendet werden, z.B. einmal wöchentlich.
Langwirksame HIV-Therapie
Als erste vollständige Therapie, die die Kriterien der „Langwirksamkeit“ erfüllt, wurde 2020 die Kombination aus Cabotegravir, einem dem Dolutegravir ähnlichen Integrasehemmer (INI), zusammen mit dem nicht-nukleosidischen Reversetranskriptase(NNRTI-)Hemmer Rilpivirin als zweimonatliche intramuskuläre Injektion in der EU zugelassen. Die Therapie kann – muss aber nicht – mit einer Phase eingeleitet werden, in der die beiden Medikamente als Tabletten (einmal täglich zu einer Mahlzeit) eingenommen werden. In dieser Phase geht es hauptsächlich darum sicherzustellen, dass die Medikamente gut vertragen werden, bevor man sie erstmalig spritzt.
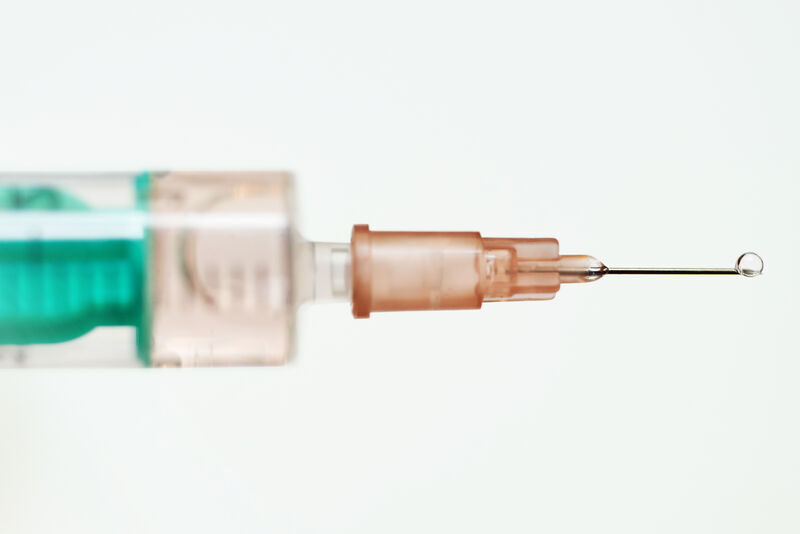
Die eigentliche „langwirksame“ Phase beginnt mit der Injektion von je einer Dosis Cabotegravir und Rilpivirin, wobei diese üblicherweise auf getrennten Seiten in die Gesäßmuskulatur (intragluteal) verabreicht werden. Dieser ersten Dosis folgt bereits nach einem Monat eine zweite, die benötigt wird, um die Konzentrationen beider Medikamente so weit „aufzusättigen“, dass sie dauerhaft in einem therapeutischen Bereich liegen. Erst danach können die Injektionen auf das zweimonatliche Erhaltungsintervall ausgeweitet werden.
Die Anwendungen müssen nicht auf den Tag genau erfolgen; ab der dritten Gabe existiert immer ein Zeitintervall von plus/minus sieben Tagen, was eine gewisse Flexibilität erlaubt. Kann eine Gabe nicht innerhalb des Zeitfensters erfolgen, so ist es möglich, die Zeit bis zur nächsten Gabe mit Tabletten zu überbrücken („Überbrückung“). Mit welchen Tabletten die Überbrückung erfolgt, kann dabei, unter Beachtung von Resistenzsituation und Wechselwirkungen (insbesondere mit Cabotegravir und Rilpivirin), frei gewählt werden. Wird das Zeitintervall um mehr als einen Monat überschritten, so muss man wieder „von vorne“ beginnen; es muss also nach der ersten Dosis nach dem verpassten Termin eine zweite Dosis bereits nach einem Monat erfolgen, bevor wieder auf eine zweimonatige Gabe umgestellt werden kann.
Für Menschen mit HIV
die sich für eine Therapie mit Cabotegravir und Rilpivirin entscheiden, gilt es zunächst zu beachten, dass durch die Injektionen vor allem an den Einstichstellen häufig unerwünschte Reaktionen wie Rötung, Schwellung, Schmerzen und blaue Flecke auftreten können. Auch systemische Nebenwirkungen kommen vor, z.B. Fieber. Sowohl in den Studien als auch in der bisherigen klinischen Erfahrung zeigt sich jedoch, dass diese Nebenwirkungen bei den meisten Menschen im Laufe der Zeit deutlich nachlassen.
Auch die erhöhte Zuzahlung ist beachtenswert: Lässt man die „Startdosis“ im ersten Jahr außer Acht, so sind pro Jahr sechs Injektionen notwendig, wobei jedes Medikament einzeln in der Apotheke abgegeben (es gibt also keine „Kombipackung“) und eine Zuzahlung von 10 Euro pro Präparat (also 20 Euro für jeden Injektionstermin) erhoben wird. Somit werden pro Jahr 120 Euro Zuzahlung fällig – statt der häufig üblichen 40 Euro (im Falle einer Ein-Tabletten-Kombination).
Insbesondere für Menschen mit langen Anfahrtswegen zu ihren HIV-Schwerpunktärzt*innen können darüber hinaus weitere Probleme entstehen, angefangen von Anfahrtszeit und -kosten bis hin zur Notwendigkeit, mehr Freizeit und ggf. Urlaubstage zu „opfern“. Auch die Verweilzeit in den Praxen und Kliniken kann etwas langer sein als gewohnt, immerhin müssen beide Substanzen nach entsprechender Vorbereitung (aufwärmen, aufziehen) gespritzt werden (wobei langsames Spritzen die Schmerzen an der Injektionsstelle zu reduzieren scheint), es vergeht Zeit durch Ent- und Ankleiden und mitunter fällt zusätzliche Wartezeit an, wenn auf die Verfügbarkeit eines Raumes gewartet werden muss.
Auch zu beachten gilt, dass nicht für jeden Menschen, der mit HIV lebt, die Kombination aus Cabotegravir und Rilpivirin in Frage kommt. Die Zulassung der Kombination schließt alle Menschen aus, bei denen in der Vergangenheit ein virologisches Versagen aufgetreten ist oder die bekannte Resistenzen im Bereich der nicht-nukleosidischen Reversetranskriptase-Hemmer (NNRTI) oder Integrase-Hemmer (INI) aufweisen.
Selbstredend müssen auch mögliche Interaktionen von Begleitmedikamenten beachtet werden. Im Falle einer gleichzeitig bestehenden Hepatitis-B-Infektion ist darauf zu achten, dass durch die Tenofovir- und Lamivudin-freie Therapie keine gleichzeitige Behandlung dieser Ko-Infektion erfolgt. Eine Behandlung ist zwar dennoch möglich, erfordert aber die zusätzliche Anwendung einer gegen Hepatitis-B wirksamen Substanz. Aus den bisher verfügbaren Studiendaten wurden zudem mögliche Risikofaktoren für ein mögliches Therapieversagen ermittelt, die neben Resistenzen, vor allem einen (bis zwei) bestimmte(n) HIV-1-Subtyp(en), sowie niedrige Arzneimittelspiegel beinhalten.
Weitere langwirksame HIV-Therapien, die versuchen, das Profil von Cabotegravir und Rilpivirin zu verbessern, sind in Entwicklung. Hierbei geht es vor allem um die Möglichkeit, die Anwendungsintervalle zu verlängern, mit kleinen Injektionsmengen auszukommen (um die Reaktionen an der Einstichstelle zu minimieren) und langwirksame Therapien auch dann zu ermöglichen, wenn bereits gewisse Resistenzen vorhanden sind. Am weitesten fortgeschritten in diesem Bemühen ist momentan wohl Lenacapavir, die erste in der EU zugelassene Substanz einer neuen Wirkstoffklasse, den sogenannten Capsid-Inhibitoren. Zugelassen ist Lenacapavir bisher als Zusatztherapie für Menschen mit HIV, die durch ausgiebige Vorbehandlung und multipler Resistenzen mit den „Standardmedikamenten“ keine ausreichende Viruskontrolle erreichen, sei es aufgrund unzureichender Wirksamkeit oder weil wirksame Substanzen nicht eingesetzt werden können (z.B. wegen Unverträglichkeit, Wechselwirkungen o.Ä.). Nach einer kurzen oralen Einleitungsphase kann die Substanz alle sechs Monate unter die Haut (subkutan) verabreicht werden.

Zu einer vollständigen Therapie, die als echter Ersatz für die konventionellen Therapien mit täglichen Tabletten dienen könnte, fehlt Lenacapavir momentan ein „Partner“, da auch Lenacapavir alleine nicht dauerhaft in der Lage ist, die HIV-Vermehrung wirkungsvoll zu unterdrücken. Der ursprünglich vorgesehene Partner Islatravir, ebenfalls erste Substanz einer neuen Klasse, der sogenannten nukleosidischen Reverse-Transkriptase-Translokations-Inhibitoren (NRTTI), wurde im Entwicklungsprogramm als ultralangwirksame Substanz aufgrund von Sicherheitsbedenken gestoppt. Das Studienprogramm ist mittlerweile zwar wieder angelaufen; die untersuchten Dosen werden sich allerdings für eine sechsmonatige Anwendung nicht eignen, könnten jedoch z.B. für eine wöchentliche Anwendung eine Rolle spielen.
Weitere Optionen, die aktuell in Aussicht stehen, sind z.B. langwirksame Formulierungen von Bictegravir und Dolutegravir (zwei als Tablette bereits mit Erfolg eingesetzte Integrasehemmer der 2. Generation), veränderte Formulierungen von Rilpivirin und Cabotegravir, neue Integrasehemmer (die z.T. bereits als Integrasehemmer der 3. Generation bezeichnet werden) und breit-neutralisierende Antikörper.
Medikamentöse HIV-Präventionsstrategien mit langwirksamen Substanzen
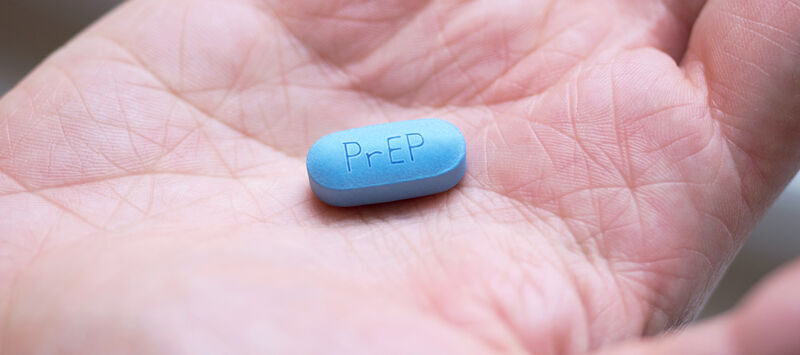
Auch in Sachen HIV-Präexpositions-Prophylaxe (HIV-PrEP) ist momentan Cabotegravir die einzig langwirksame zugelassene Substanz, die jedoch bisher nur in wenigen Ländern tatsächlich zur Verfügung steht bzw. angewandt wird. In Europa existiert bislang nur eine formale EU-Zulassung; die Markteinbringung als PrEP ist noch nicht erfolgt. Auch andere langwirksame Substanzen aus dem Repertoire der HIV-Therapie werden zur Anwendung als PrEP untersucht.
Ausblick
Für Prophylaxe und Therapie werden neben neuen Präparaten auch neue Anwendungsformen auf uns zukommen. So werden für die genannten Optionen neben subkutaner und intramuskulärer Anwendung auch die direkte intravenöse Gabe, also als Infusion, notwendig, und subdermale Implantate, mit und ohne die Möglichkeit, diese nachzufüllen, stehen immer wieder zur Diskussion. Besonders die subkutane Gabe erscheint vielfach als interessante Option, weil sie prinzipiell die Möglichkeit zur Selbstanwendung mit sich bringen könnte.
Neben all den theoretischen Möglichkeiten wird ganz praktisch eine Rolle spielen, welche der genannten Strategien in Deutschland überhaupt auf den Markt kommen werden. Unter den oben beschriebenen Optionen hat sich der Patentinhaber von Lenacapavir, Gilead Sciences, bereits gegen eine Vermarktung in Deutschland entschieden, (zumindest in der aktuellen Indikation), und auch der PrEP mit Cabotegravir wird in Deutschland momentan keine Zukunft prophezeit, solange keine generische Verfügbarkeit besteht. Grund ist die für die Vertreibenden unattraktive Vergütung auf dem Boden der aktuellen Preisfindungsverfahren.
Zum Autor:

Dr. med. Sebastian Noe ist Facharzt für Innere Medizin und Endokrinologie und Diabetologie, seit 2015 im MVZ München am Goetheplatz tätig, Vorstandsmitglied der DAIG e.V.
Hier findest du weitere Artikel und Informationen auf unseren anderen Seiten
- Grundlegende Informationen zu Therapie auf aidshilfe.de: HIV-Behandlung
- Weiterführender Artikel auf magazin.hiv: HIV-Therapie: Neue Ansätze und Entwicklungen
- Grundlegende Informationen zu Prävention auf aidshilfe.de: Safer Sex
- Weiterführender Artikel auf magazin.hiv: Impfung gegen HIV – wo stehen wir?
Diesen Beitrag teilen






